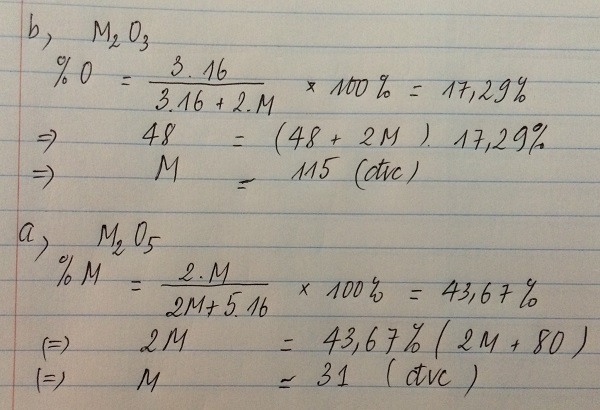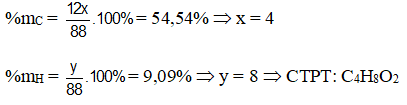1 h/c của phi kim A (hoá trị V) vs oxi . Bt%theo khối lượng A là 43,67% còn lại là oxi. tìm CTHH của h/c

Những câu hỏi liên quan
a. Oxit của một nguyên tố hóa trị V chứa 43,67% nguyên tố đó. Xác định CTHH
b. Oxit của một nguyên tố hóa trị III chứa 17,29% O . Xác địnhCTHH
c. Oxit của một nguyên tố hóa trị IV chứa 13,4% khối lượng oxi. Xác định CTHH
Làm lại nhé
Câu a: Gọi công thức oxit là A2O5 (Kí hiệu A trùng với nguyên tử khối ở dưới nhé)
Theo đề ra ta có:
\(\frac{2.A}{2.A+16.5}=\frac{43,67}{100}\). Giải phương trình ta được A = 31
=> CTHH là \(P_2O_5\)
Ủng hộ mình nha
Đúng 0
Bình luận (0)
a) Gọi A là nguyên tố hóa trị V
CTTQ: A2O5
Ta có: %(m)O = 100 - 43,67 = 56,33 (%)
Ta lại có: \(\frac{m_A}{m_O}=\frac{\%m_A}{\%m_O}\) ⇔ \(\frac{2A}{5.16}\) = \(\frac{43,67}{56,33}\)
⇔ 2A = \(\frac{80.43,67}{56,33}\) \(\approx\) 62 ⇒ A = 31 (đvC)
Vậy nguyên tố A là Photpho (P)
CTHH: P2O5
b) Gọi B là nguyên tố hóa trị III
CTTQ: B2O3
Ta có: %(m)B = 100 - 17,29 = 82,71 (%)
Ta lại có: \(\frac{m_B}{m_O}\) = \(\frac{\%m_B}{\%m_O}\) ⇔ \(\frac{2B}{48}\) = \(\frac{82,71}{17,29}\)
⇔ 2B = \(\frac{48.82,71}{17,29}\) \(\approx\) 230 ⇒ B = 115 (đvC)
Vậy B là nguyên tố Indium (Indi)
CTHH: Indi2O3
Continute
Chúc bạn học tốt!!!
Vậy nguyên tố A là Photpho (P)
Đúng 0
Bình luận (0)
1,Đốt cháy hoàn toàn 1,36g hợp chất x sinh ra 0,896l SO2 (đktc) và 0,72 g H2O Bt tỉ khối của x đối vs NH3= 2. Xác định CTHH của x.
2,Xác định CTHH của hợp chất RH3. bt trong hợp chất của R hóa trị V có chứa 56,34% oxi theo khối lượng.
Giúp mình vs, cảm ơn trước!
1)
X+O2->SO2+H2O
Vì sản phẩm có các nguyên tố S,H,O nên X gồm có các nguyên tố S;H và có thể có O
\(n_{SO_2}\)=0,896:22,4=0,04(mol)
=>nS(X)=\(n_{SO_2}\)=0,04(mol)=>mS(X)=0,04.32=1,28(g)
\(n_{H_2O}\)=0,72:18=0,04(mol)
=>nH(X)=2\(n_{H_2O}\)=0,04.2=0,08(mol)
=>mH(X)=0,08.1=0,08(g)
=>mS(X)+mH(X)=0,08+1,28=1,36(g)=mX
=>Trong X không có O
Gọi CTTQ hợp chất X là:HxSy
x:y=\(\dfrac{0,08}{1}\):\(\dfrac{1,28}{32}\)=2:1
Gọi CTĐG X là:H2S=>CTN X là:(H2S)n
Mặt khác:Mx=\(M_{NH_3}\).2=17.2=34
=>34n=34=>n=1
Vậy CTHH X là:H2S
Đúng 1
Bình luận (1)
1 oxit kim loại X có hóa trị VI chứa 48% oxi theo khối lượng
a) xác đinh tên của X
b) CTHH của oxit
Bài 1: Khối lượng kim loại R trong muối Cacbonat chiếm 40%. Xác định CTHH của muối cacbonat,biết R có hóa trị II không đổi.
Bài 2: Oxi của một nguyên tố R ở mức hóa trị thấp chứa 39.36% nguyên tố Oxi về khối lượng. Cũng oxit của nguyên tố đó ở mức hóa trị cao chứa 74.07% Oxi về khối lượng .Tìm CTHH của 2 oxit
Bài 1:
gọi cthh của muối cần tìm là RCO3
theo bài ra ta có : %RRCO3 = 40% => %gốc CO3 RCO3=60%
=> MRCO3 = MCO3 : 60% = 60 : 60% = 100
=> MR =100 - 60 = 40 => R là Ca => CaCO3
Đúng 0
Bình luận (0)
Câu 4: Hợp chất A chứa 40% khối lượng nguyên tố lưu huỳnh, còn lại là nguyên tố oxi. Biết M h/c = 80 gam / mol. Tìm CTHH và cho biết tên của hợp chất A đó.
mS = 80 . 40% = 32 (g)
nS = 32/32 = 1 (mol)
mO = 80 - 32 = 48 (g)
nO = 48/16 = 3 (mol)
CTHH: SO3
Đúng 2
Bình luận (0)
mS = 80 . 40% = 32 (g)
nS = 32/32 = 1 (mol)
mO = 80 - 32 = 48 (g)
nO = 48/16 = 3 (mol)
CTHH: SO3
chúc bn học tốt ![]()
Đúng 0
Bình luận (0)
a, Tìm CTHH của một oxit của nito. Biết rằng trong oxit này có 7g N kết hợp 16g O. khí này nặng hơn khí oxi bao nhiêu lần?
b,Một hợp chất có thành phần % về khối lượng các nguyên tố : 70% Fe, 30%O. Hãy xác định CTHH của hợp chất đó.
c. Hợp chất giữa nguyên tố X với O có %X43,67% về khối lượng. Biết X có hóa trị V trong hợp chất với oxi. Tìm X và viết CTHH của hợp chất trên.
Đọc tiếp
a, Tìm CTHH của một oxit của nito. Biết rằng trong oxit này có 7g N kết hợp 16g O. khí này nặng hơn khí oxi bao nhiêu lần?
b,Một hợp chất có thành phần % về khối lượng các nguyên tố : 70% Fe, 30%O. Hãy xác định CTHH của hợp chất đó.
c. Hợp chất giữa nguyên tố X với O có %X=43,67% về khối lượng. Biết X có hóa trị V trong hợp chất với oxi. Tìm X và viết CTHH của hợp chất trên.
Gỉa sử CTHH là FexOy, ta có tỉ lệ:
\(\dfrac{x}{y}\)=\(\dfrac{70}{56}\):\(\dfrac{30}{16}\)=\(\dfrac{2}{3}\)⇒CTHH là Fe2O3
Đúng 1
Bình luận (0)
Gọi CTHH của hợp chất là X2O5, ta có:
%X=\(\dfrac{2X}{2X+16.5}\)100%=43,67%⇒ X = 31⇒X là P
⇒CTHH của hợp chất: P2O5
Đúng 1
Bình luận (0)
Gọi CTHH của hợp chất là X2O5, ta có:
%X=2X2X+16.52X2X+16.5100%=43,67%⇒ X = 31⇒X là P
⇒CTHH của hợp chất: P2O5
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
hợp chất X có chứa 54,54%C, 9,09%H và còn lại là nguyên tố oxi về khối lượng. Tỉ khối của T so với H2 bằng 44. Tìm CTHH của hợp chất T
Câu 1 Xác định công thức phân tử của oxit sắt biết nồng độ % theo khối lượng của Fe=70% còn lại là oxi Câu 2 cho biết nồng độ % theo khối lượng của các chất trong oxit là Al=52,94% còn lại là oxi Xác định công thức phân tử Câu 3 tìm CTHH của 1 oxit biết tỉ lệ về khối lượng là \(\dfrac{m_N}{m_O}\)=\(\dfrac{7}{12}\)
Câu 1 :
\(CT:Fe_xO_y\)
\(\%O=100-70=30\%\)
\(\dfrac{\%Fe}{\%O}=\dfrac{56x}{16y}=\dfrac{70}{30}\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
\(CT:Fe_2O_3\)
Đúng 2
Bình luận (0)
Câu 2 :
\(CT:Al_xO_y\)
\(\%O=100-52.94=47.06\%\)
Ta có :
\(\dfrac{27x}{16y}=\dfrac{\%Al}{\%O}=\dfrac{52.94}{47.06}\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
\(CT:Al_2O_3\)
Đúng 3
Bình luận (0)
Câu 3 :
\(CT:N_xO_y\)
Ta có :
\(\dfrac{m_N}{m_O}=\dfrac{7}{12}\Rightarrow\dfrac{14x}{16y}=\dfrac{7}{12}\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
\(CT:N_2O_3\)
Đúng 3
Bình luận (0)
Xem thêm câu trả lời
oxit của 1 nguyên tố X có hóa trị là 5. biết X chiếm 43,67% về khối lượng, còn lại là phần trăm của oxi. tì công thức phân tử và tnhs PTK của oxit trên
CTDC của oxit: X2O5
Ta có:
\(\frac{2X}{2X+5.16}=\frac{43,67}{100}\\\Leftrightarrow\frac{2X}{2X+80}=0,4367 \\ \Leftrightarrow2X=0,8734X+34,936\\ \Leftrightarrow1,1266X=34,936\\ \Leftrightarrow X=31\)
Vậy X là Photpho (P)
Công thức phân tử là: P2O5
PTK của oxit là: 2.31 + 5.16 = 142
Đúng 0
Bình luận (0)
A là một hợp chất của nguyên tố R với oxi. Biết R là nguyên tố phi kim có hoá trị V và tỉ khối của A so với khí hiđro là 54. Hãy xác định công thức hoá học của A.
(Biết: O = 16, N = 14, C = 12, CI = 35,5)
CTHH: R2O5
MA = 54.2 = 108(g/mol)
=> 2.MR + 16.5 = 108
=> MR = 14(N)
=> CTHH: N2O5
Đúng 2
Bình luận (0)